Poznajmy się

Paweł Kruś ?Świat lekarza?
Bardzo się cieszymy, że sojusz Strefy Inwestorów i ?Świata Lekarza? został tak życzliwie przyjęty przez naukowców prowadzących innowacyjne badania dla zdrowia, inwestorów i firmy biotechnologiczne oraz agendy państwowe odpowiedzialne za rozwijanie nowoczesnej gospodarki. Wypowiedź prof. Macieja Chorowskiego, prezesa NCBiR, uświadomiła realia zaangażowania rządu w nasz sektor. Ukazała się w poprzednim wydaniu.
Dziś robimy kolejne kroki milowe ? gościmy polskich liderów firm biotechnologicznych, wsród nich ? prezesa Biotonu Roberta Neymanna, który zadziwił giełdę w pierwszym półroczu nową wyceną i stabilnością notowań akcji swojej Firmy. Bardzo chcieliśmy go wam przedstawić.
Najgorsze jest nieznane ? wiemy o tym wszyscy. Dlatego zapraszamy na łamy wszystkie spółki biotechnologiczne, telemedyczne i produkujące najnowocześniejszy sprzęt do szpitali i klinik. Poznajmy się, będzie łatwiej rozmawiać o wspólnych przedsięwzięciach.
Trzeci Raport o spółkach biotechnologicznych ?Świata Lekarza? i Strefy Inwestorów ukaże się w grudniu.
Paweł Kruś
 Paweł Biedrzycki
Paweł Biedrzycki
Strefa Inwestorów
Miejsce polskiej biotechnologii
Od lipca 2018 r., kiedy opublikowaliśmy pierwszy raport na temat biotechnologii, w samej branży i na giełdzie dużo się wydarzyło. Pogorszenie koniunktury na rynku giełdowym wywiera presję także na notowania akcji spółek biotechnologicznych. Sektor tym negatywnym tendencjom się skutecznie opiera. Problem mają jednak te firmy biotechnologiczne, które nie pozyskały jeszcze kapitału na rozwój.
W tej chwili w sektorze ma miejsce bardzo ciekawa sytuacja. Z jednej strony spółki biotechnologiczne mogą liczyć na wiele publicznych grantów badawczych na sfinansowanie prowadzonych przez siebie projektów. Z drugiej strony, brakuje prywatnego kapitału, który sfinansowałby wkład własny do ich realizacji. To duże wyzwanie dla sektora, tym bardziej że wszystko wskazuje na to, że sztandarowy program NCBiR, wspierający innowacyjne projekty, czyli Bridge Alfa, zostanie poważnie okrojony. Z początkowych 3 mln zł wartość inwestycji funduszu nie będzie mogła przekraczać 1 mln zł. To znacząco ogranicza sensowność prowadzenia tego rodzaju działalności po stronie Towarzystw Funduszy Inwestycyjnych. Co za tym idzie, przynajmniej na jakiś czas, dostęp do finansowania dla projektów biotechnologicznych może zostać ograniczony. Niektóre firmy, w początkowej fazie rozwoju, mogą mieć problemy z dalszym postępem badań.
Równolegle, największe firmy biotechnologiczne osiągają znaczne postępy. W ciągu ostatnich trzech miesięcy sporo się wydarzyło. Selvita ostatecznie przekazała dalsze prace nad badaniami klinicznymi nad projektem SEL24 włoskiej spółce Menarini. Celon Pharma zakończyła pierwszą fazę badań klinicznych nad esketaminą i otrzymała pozwolenie na rozpoczęcie drugiej fazy badań. Mabion złożył wniosek rejestracyjny dla Mabion CD20 do Europejskiej Agencji Leków ? EMA.
Rejestracja produktów biotechologicznych

Barbara Jaworska-Łuczak, Wiceprezes ds. Produktów Biobójczych, URPLWMiPB
Obecnie przemysł biotechnologiczny postrzegany jest jako jeden z najszybciej rozwijających się sektorów gospodarki wysokich technologii. Innowacyjne rozwiązania wprowadzają istotne zmiany we właściwościach wielu różnych produktów, począwszy od kosmetyków, poprzez żywność (w tym m.in. suplementy diety, żywność specjalnego przeznaczenia medycznego itd.), produkty biobójcze, środki ochrony roślin, aż po najnowocześniejsze technologie medyczne obejmujące zarówno wyroby, jak i produkty lecznicze. Rozwiązania te powodują powstawanie również swoistego rodzaju nowej nomenklatury, jak np. nutraceutyki czy kosmeceutyki, które powodują pewnego rodzaju trudności rejestracyjne, ponieważ nie funkcjonują one w obowiązujących aktach prawnych, a co za tym idzie, znacząco wydłuża się czas możliwości wprowadzenia ich do obrotu.
W Polsce powstało wiele interesujących projektów naukowych, w wyniku których opracowano produkty biotechnologiczne o różnych właściwościach prozdrowotnych. Jednak w toku prac nad przygotowaniem wielu z tych projektów ich autorzy nie wzięli pod uwagę bardzo ważnego aspektu, który stanowi o możliwości komercjalizacji tychże produktów, a mianowicie o ich rejestracji, pozwalającej na legalne wprowadzenie do obrotu. W zależności od ich statusu, produkty są rejestrowane w różny sposób, jednak zawsze wymaga to znajomości przepisów prawa, nakładów finansowych oraz czasu. Trzeba także pamiętać o wymaganiach rejestracyjnych dotyczących stosownych badań. Reasumując, w przypadku projektowania nowych produktów biotechnologicznych trzeba bezwzględnie brać pod uwagę kwestie ich rejestracji, która pozwoli na ich komercjalizację.
Chcemy być specjalistyczną firmą z obszaru biotechnologii i diabetologii

Rozmowa z prezesem zarządu Bioton S.A. ? Robertem Neymannem.
Panie Prezesie ? na początek krótka historia ? jak Pana drogi przecięły się z drogą Biotonu?
W zeszłym roku w maju Rada Nadzorcza powołała mnie w skład zarządu spółki, powierzając mi funkcję prezesa. Zainteresowałem przedstawicieli akcjonariuszy swoją wizją uporządkowania bieżących spraw spółki i klarowną strategią jej rozwoju. Jak sądzę, także moje dotychczasowe doświadczenie w restrukturyzacji i rozwijaniu firm miało tu znaczenie. Chyba również to, że przyszedłem z wydawałoby się odległego od przemysłu farmaceutycznego sektora FMCG. Myślę, że te elementy i właśnie to spojrzenie i nieszablonowe podejście pozwalają mi dziś na ukierunkowanie wysiłków spółki na pokonywanie trudności, wdrażanie standardów, stawianie i realizację celów.
Spółka Bioton to niezwykle ciekawa polska, nowoczesna firma biotechnologiczna, do niedawna nieco może przykurzona i ?po przejściach?, ale mająca unikatową wiedzę i kompetencję w produkcji insuliny. Takich liczących się na świecie firm jest zaledwie 10. Jest to elitarny klub. Pomyślałem, przychodząc tutaj i znając czekające mnie zadania, że to niezwykle ciekawe wyzwanie menedżerskie, a jednocześnie możliwość zrobienia czegoś dobrego ? produkujemy przecież leki ratujące życie i poprawiające jego standard.
Co ważnego dzieje się zatem w Biotonie, jakie są najbliższe plany i cele, jak wyglądają plany inwestycyjne?
Najważniejsze w ostatnim roku było uporządkowanie spraw finansowych i organizacyjnych spółki. W tym pierwszym obszarze ograniczyliśmy chociażby tzw. kapitał pracujący do kwoty 54 mln zł na koniec 2017 roku wobec 100 mln zł w maju 2017 roku. Co więcej, mogę już powiedzieć, że poziom kapitału pracującego prawdopodobnie spadnie do blisko zera na koniec tego roku. To bardzo odciąża spółkę i stawia ją na bezpiecznej pozycji, jeśli chodzi o przepływy pieniężne.
W 2017 roku poprawiliśmy też wydajność produkcji insuliny ludzkiej o prawie 100 proc., co wpłynęło m.in. na redukcję kosztów. Mamy jednak apetyt na więcej. Zakładam, że w ciągu kolejnego roku uda się poprawić wydajność o dalsze około 20 proc.
Chcemy być specjalistyczną firmą z obszaru biotechnologii i diabetologii. Nasza strategia koncentruje się na trzech obszarach, które nazywamy Zintegrowanymi Rozwiązaniami Diabetologicznymi, w którego skład wchodzą: leki, urządzenia i usługi. Przyszłość Biotonu to przede wszystkim produkcja insuliny (udział Biotonu w polskim rynku insuliny ludzkiej wynosi 33 proc.), jak również te produkty i rozwiązania, które pomagają w terapii pacjentowi diabetologicznemu, czyli m.in. urządzenia diagnostyczne, narzędzia monitorujące terapię.
Oprócz insuliny ludzkiej, której produkcję i sprzedaż rozwijamy od lat, pracujemy nad analogami insuliny. Analogi insulin to docelowo strategiczna pozycja, bardzo ważna w naszym portfelu. Obecnie mamy opracowane analogi, skalujemy je do produkcji przemysłowej, następnie czeka nas proces rejestracji poprzedzony badaniami przedklinicznymi i klinicznymi. Cały proces zajmie 4-5 lat. Do tego czasu chcemy rozwijać sprzedaż insuliny ludzkiej, zwłaszcza na rynkach zagranicznych.
Z kolei, co do porządkowania struktury firmy, ostatnio przeprowadziliśmy proces sprzedaży spółki dystrybucyjnej w Singapurze ? środki uzyskane ze sprzedaży jej akcji wpłynęły już do spółki. 32,5 mln zł przeznaczyliśmy na spłatę zadłużenia, co znacząco poprawiło naszą sytuację i pomogło obniżyć koszty finansowe. Reszta środków zostanie przeznaczona na rozwój sprzedaży insulin ludzkich oraz proces badań i rejestracji analogów. To teraz nasz najważniejszy cel, którego osiągnięcie postawi Bioton w szeregu kluczowych producentów insulin na świecie. Wierzę, że to realne i że osiągniemy ten cel w ciągu najbliższych 4-5 lat.
Rozmawiała Maria Wójcik
Bioton (GPW)
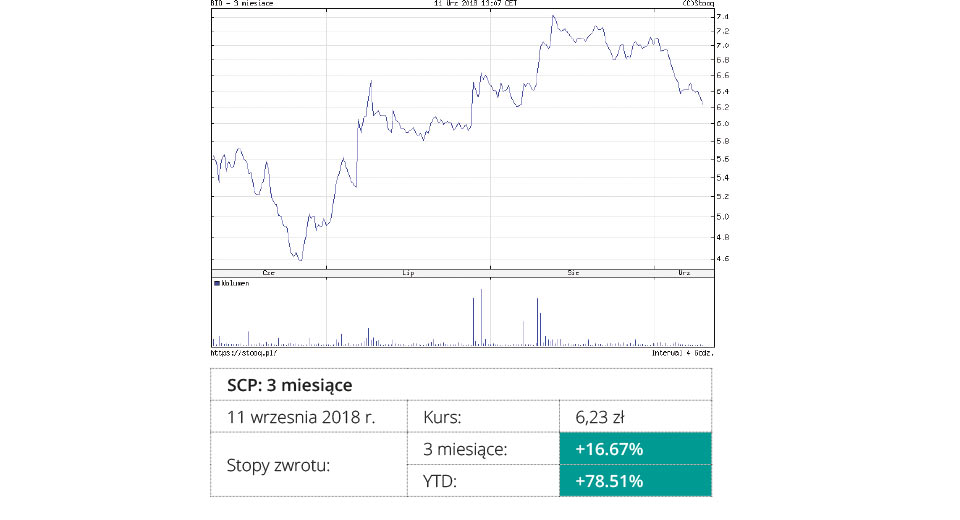
Wartość rynkowa: 428 mln zł
Przychody: 366,2 mln zł
Zyski: 5,5 mln zł
Stan gotówki: 31 mln zł
Najważniejsze wydarzenia: Bioton to najstarsza spółka z sektora biotechnologicznego na polskiej giełdzie. Producent insuliny ludzkiej, którą sprzedaje w Europie i Azji. W tej chwili spółka prowadzi dwa projekty, których celem jest stworzenie insuliny analogowej. Obydwie insuliny Bioton planuje zarejestrować na trzech rynkach (Europa, USA i świat). Kluczowym wydarzeniem w pierwszej połowie 2018 roku była sprzedaż spółki zależnej z Azji odpowiadającej za dystrybucję leków, za co Bioton otrzymał ponad 100 mln zł.
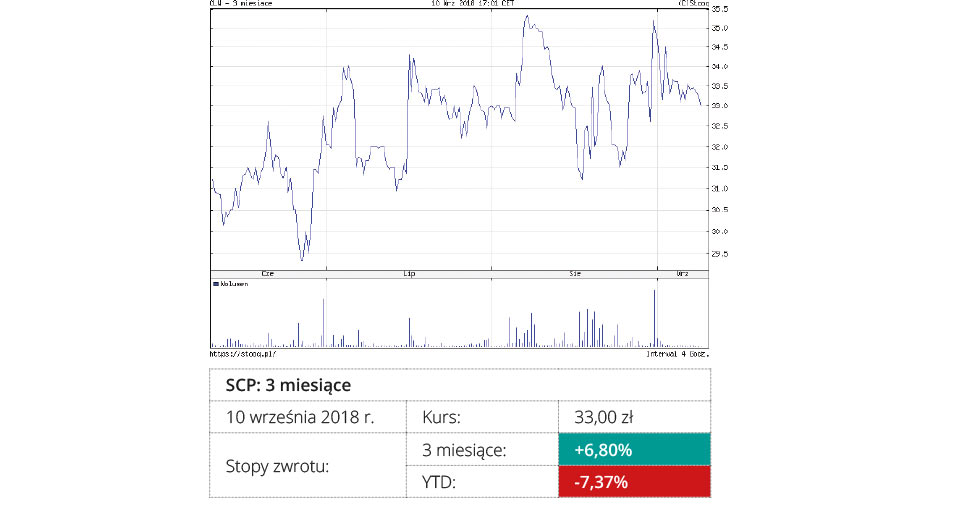
Scope Fluidics złożył wniosek patentowy
Scope Fluidics S.A. ? notowana na NewConnect spółka biotechnologiczna będąca właścicielem innowacyjnych projektów z zakresu diagnostyki medycznej ? złożyła wniosek do Europejskiego Urzędu Patentowego (EPO) o ochronę technologii wykorzystanej w systemie Bacteromic, służącej do szybkiego badania lekowrażliwości mikroorganizmów. Uzyskanie europejskiego patentu na wynalazek spółki będzie chronić system Bacteromic oferujący nie tylko zdecydowanie bardziej kompleksową, ale potencjalnie również szybszą analizę antybiotykowrażliwości, niż produkty konkurencyjne.
Rozwiązania, o których opatentowanie ubiega się spółka, wspierają badanie metodą fenotypową ? stanowiącą złoty standard wiarygodności w diagnostyce medycznej, przy tym znacząco skracając czas hodowli bakterii potrzebny do wykrycia ich wzrostu i oznaczenia poziomu oporności na dany antybiotyk. Technologia zastosowana w systemie Bacteromic umożliwia wyjątkowo kompleksową analizę próbki ? uzyskanie z jednego testu ilościowego antybiogramu, dla wszystkich klinicznie stosowanych antybiotyków. Ponadto użyte rozwiązania są kompatybilne z ekonomicznymi metodami w konstrukcji analizatorów diagnostycznych.
Wniosek do Europejskiego Urzędu Patentowego o zastrzeżenie technologii wykorzystywanej w systemie Bacteromic został złożony w połowie lipca, by chronić metodę zbierania i analizy danych, umożliwiającą bardzo szybkie oznaczanie poziomu stężenia antybiotyku, które hamuje wzrost bakterii. Wraz z dwoma poprzednimi zgłoszeniami patentowymi, złożonymi w marcu tego roku, tworzy ono pakiet pokrywający kluczowe technologie, stanowiące o przewadze analizatora Bacteromic nad konkurencyjnymi systemami diagnostycznymi.
Scope Fluidics
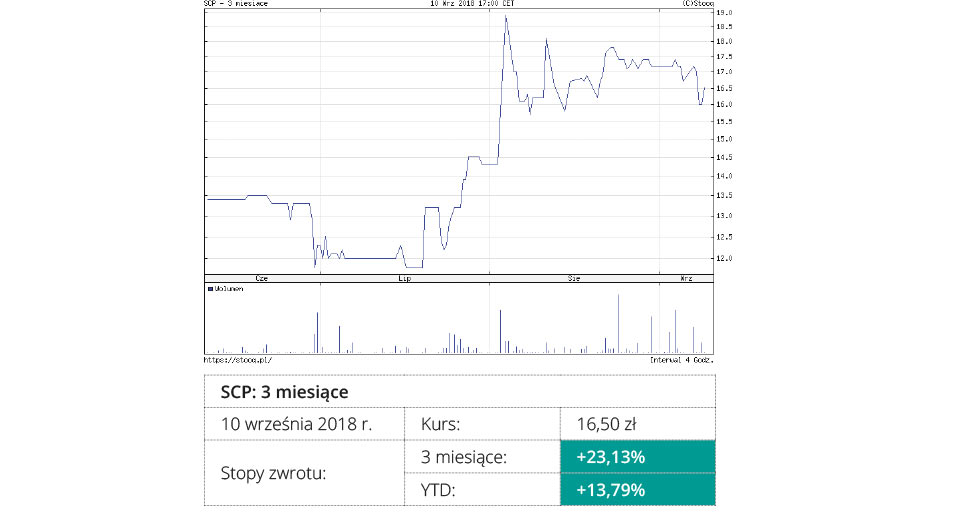
Spółka prowadzi prace nad dwoma projektami z obszaru medtech: PCR|ONE i bacteromic. Obecnie bliższy komercjalizacji jest system PCR|ONE, czyli urządzenie, które ma zapewnić najszybsze na świecie wykrywanie bakterii i wirusów.
Projekt PCR|ONE jest w procesie industrializacji i wchodzi w fazę produkcji pilotażowej. Na początku 2018 r. Spółka podpisała umowę o współpracy z ogólnopolską siecią laboratoriów diagnostycznych ALAB. Natomiast proces komercjalizacji PCR|ONE będzie wspierany przez czołową międzynarodową firmę doradczą Clairfield International, która jest odpowiedzialna za strategię sprzedaży systemu PCR|ONE oraz poszukiwanie nabywcy. Komercjalizacja PCR|ONE ma nastąpić najpóźniej w pierwszej połowie 2020 r. Do połowy 2018 r. system PCR|ONE kosztował ok. 10 mln zł. Spółka przewiduje, że całościowe wydatki wyniosą ok. 20 mln zł. Projekt został dofinansowany środkami z programu Eureka i NCBiR.
NEUCA znacząco zwiększa zyski i zacieśnia współpracę z aptekami
Spółka w pierwszej połowie 2018 r. wypracowała blisko 51,7 mln zł zysku netto bez zdarzeń jednorazowych, czyli o 10 proc. więcej niż w analogicznym okresie 2017 roku. W samym drugim kwartale br. NEUCA zarobiła 18,5 mln zł netto, co oznacza wzrost o 58 proc. Jednocześnie Grupa osiągnęła wysoką marżę brutto na poziomie 10,72 proc., czyli o 1,21 p.p. więcej wobec drugiego kwartału 2017 r.
NEUCA w pierwszych sześciu miesiącach 2018 r. odnotowała wzrost przychodów o ponad 4 proc. do 3,94 mld zł. Jednocześnie Grupa zachowała silną pozycję rynkową, osiągając blisko 29 proc. udziałów w branży hurtu aptecznego.
Sprzedaż produktów własnych do aptek wzrosła w pierwszych sześciu miesiącach o 22 proc. do 72 mln złotych. W sumie w tym czasie apteki sprzedały 19,5 mln produktów z portfolio Synoptis Pharma, a NEUCA osiągnęła 17,5 mln zł zysku netto, czyli o 14% więcej niż przed rokiem. Grupa intensywnie rozwija współpracę z farmaceutami w ramach programów aptecznych. Na koniec pierwszego półrocza 2018 r. uczestniczyło w nich ponad 5700 aptek (42 proc. aptek w kraju), w tym w programie Partner+ 805 aptek (6 proc. krajowych aptek).
NEUCA w ostatnim półroczu dużo uwagi poświęciła poprawie jakości serwisu i pracy nad satysfakcją klienta. Wynik tej pracy obrazuje wysoki poziom wskaźnika NPS (Net Promotor Score), który w drugim kwartale osiągnął rekordowy poziom 38 punktów. Systematyczne działania związane z tym obszarem mają przełożenie na silną pozycję Grupy wśród aptek niezależnych. W pierwszym półroczu udziały rynkowe w tym segmencie sięgnęły 31 proc. Dodatkowy wpływ na miejsce Spółki na rynku ma rozszerzanie zasięgu programów aptecznych i rynkowych aktywności. Na koniec czerwca uczestniczyło w nich ponad 5700 aptek, tj. już 42 proc. działających w kraju.
Selvita
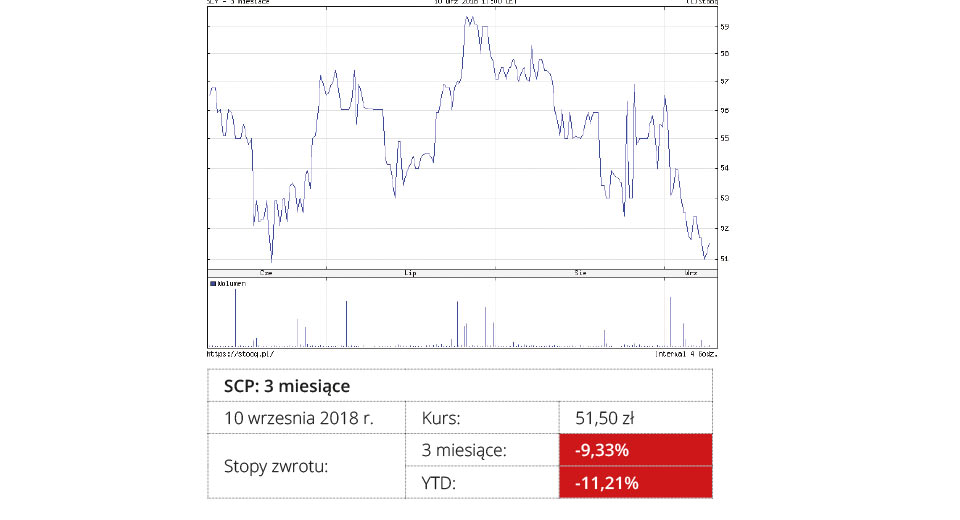
Selvita ma pipeline kilkunastu projektów innowacyjnych, ale dwa z nich, ze względu na stopień zaawansowania, są kluczowe. Pierwszy to SEL24, potencjalny nowy lek na ostrą białaczkę szpikową. Na początku 2017 r. został zakupiony przez włoską Menarini Group i w połowie 2018 r. partner przejął w pełni dalszy rozwój projektu. SEL24 jest obecnie badany w kilku ośrodkach w Stanach Zjednoczonych w ramach I fazy badań klinicznych.
Drugim flagowym projektem spółki jest SEL120, który ma potencjał w leczeniu ostrej białaczki szpikowej oraz guzów litych. W I kwartale 2019 r. spółka planuje wprowadzić go do badań klinicznych w Stanach Zjednoczonych. W projekt SEL120 zainwestowane zostało już około 30 mln zł. Planowane wydatki w najbliższych czterech latach to 70 mln zł. Strategicznym partnerem w projekcie jest największa na świecie fundacja wspierająca walkę z nowotworami układu krwiotwórczego ? Leukemia & Lymphoma Society.
SEL24 został licencjonowany w marcu 2017 r. do włoskiej grupy farmaceutycznej Menarini. Wartość płatności z góry wyniosła 20 mln zł, a potencjalna wartość umowy, wliczając wszystkie kamienie milowe oraz refundację kosztów badań i ochrony patentowej, może wynieść nawet około 400 mln zł. Do tego dochodzą potencjalne tantiemy od sprzedaży ? w przypadku, w którym SEL24 trafiłby kiedyś na rynek.
SEL120 znajduje się w ostatniej fazie badań przedklinicznych. Planowane jest wejście do kliniki na początku 2019 r. Zgodnie z przedstawioną przez Selvitę strategią na lata 2017-2021, SEL120 będzie komercjalizowany w znacznie bardziej zaawansowanej fazie rozwoju niż dotychczasowe projekty. Mowa o fazie IIa badań klinicznych, a więc po wstępnym określeniu skuteczności terapeutycznej. Spółka liczy w związku z tym na znacznie wyższe wpływy ze sprzedaży projektu niż w przypadku SEL24.
OncoArendi Therapeutics
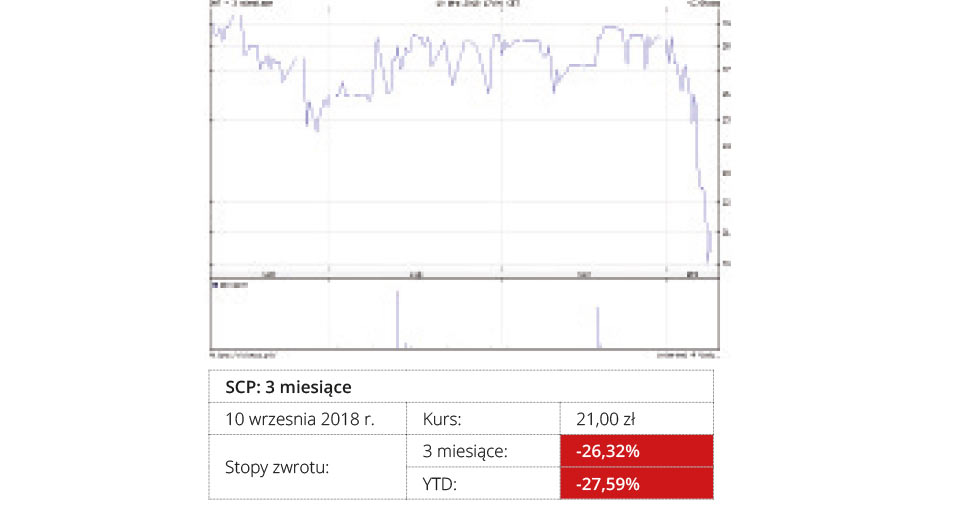
Najbardziej zaawansowanym projektem OncoArendi jest rozwój kliniczny cząsteczki OATD-01 do zastosowania w leczeniu chorób układu oddechowego. Potencjalne zastosowania lecznicze OATD-01 to choroby rzadkie, takie jak sarkoidoza czy idiopatyczne włóknienie płuc, jak również wybrane grupy pacjentów cierpiących na sterydooporną astmę oskrzelową. Profil farmakologiczny OATD-01 pozwala sądzić, że będzie to lek podawany w formie tabletki raz dziennie.
W marcu tego roku zakończone zostały badania kliniczne typu ?First in Human? (faza Ia, jednokrotnego podania rosnącej dawki leku grupie zdrowych ochotników). Późną jesienią tego roku spółka planuje rozpocząć badania fazy klinicznej Ib, w której przeprowadzona zostanie ocena bezpieczeństwa i farmakokinetyki związku przy wielokrotnym podaniu go zdrowym ochotnikom w trzech różnych dawkach. Zakończenie fazy badań Ib planowane na wiosnę 2019 r.
We wskazaniach terapeutycznych, trudniejszych pod względem rekrutacji pacjentów lub skali badania, OncoArendi zamierza przeprowadzić badania kliniczne już we współpracy z większym partnerem czy wręcz sprzedać prawa do cząsteczki w formie licencji dużej firmie farmaceutycznej. Są duże szanse na podpisanie pierwszej umowy partneringowej w perspektywie najbliższych kilkunastu miesięcy.
Łączne nakłady na badania przedkliniczne i kliniczne OATD-01 wyniosły ok. 34 mln zł, z czego ponad 21 mln zł to środki pozyskane z dotacji publicznych, a 12,5 mln zł ? wkład własny spółki.
Medicalgorithmics
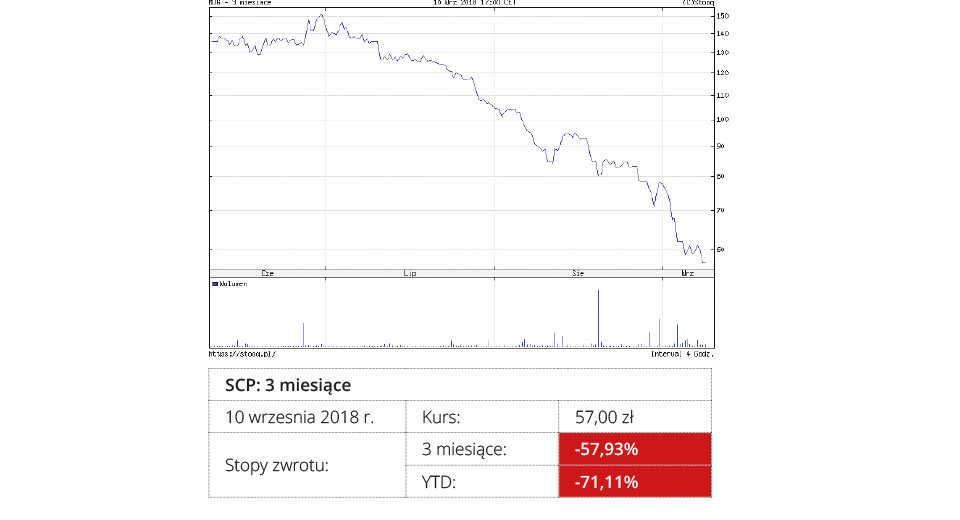
Spółka obecnie skupia się na rozwoju projektu ECG TechBot, który ma umożliwić pełną automatyzację weryfikacji analizy i interpretacji badania EKG. Zestaw opracowanych algorytmów pozwoli na weryfikację analizy rytmu serca i klasyfikację morfologii. Zmniejszy to ryzyko błędów ludzkich przy weryfikacji analizy sygnału EKG oraz zoptymalizuje pracę centrum monitoringu. Spółka planuje implementację oprogramowania ECG TechBot w kluczowym produkcie ? PocketECG (system diagnostyczny do wykrywania arytmii serca) oraz we wszystkich innych własnych rozwiązaniach z zakresu telemetrii kardiologicznej. Projekt jest w fazie badań przemysłowych. Przejście do fazy prac rozwojowych jest spodziewane za mniej więcej 2-3 lata, a zakończenie prac w 2022 r. Później planowane jest wdrożenie i komercjalizacja prac R&D. Projekt ma budżet w wysokości 11,2 mln zł i otrzyma dofinansowanie w wysokości 6,3 mln zł z NCBiR.
Synektik
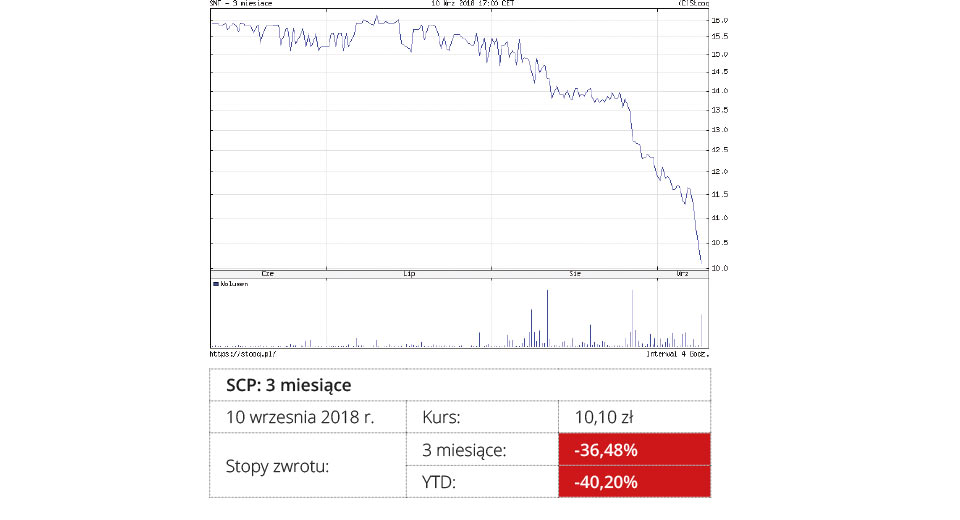
Spółka skupia się na rozwoju kardioznacznika ? innowacyjnego w skali światowej radiofarmaceutyku do badania perfuzji mięśnia sercowego. Kardioznacznik ma umożliwić dokładną diagnostykę choroby wieńcowej przy wykorzystaniu pozytonowej tomografii komputerowej (PET/CT).
Obecnie spółka jest na etapie II fazy badań klinicznych kardioznacznika i spodziewa się jej zakończenia w 2018 r. Kardioznacznik ma potencjalne zastosowanie globalne. Strategicznym rynkiem w przypadku kardioznacznika będą Stany Zjednoczone. Wydatki na realizację I i II fazy badań klinicznych zostały pokryte środkami z bezzwrotnej, niewymagającej wkładu własnego dotacji w wysokości 15,7 mln zł otrzymanej z programu Horyzont 2020. Dodatkowo Synektik otrzymał grant pozyskany z NCBiR w wysokości ponad 5,3 mln zł. Spółka nie zdecydowała jeszcze o sposobie finansowania III fazy klinicznej.
NanoGroup
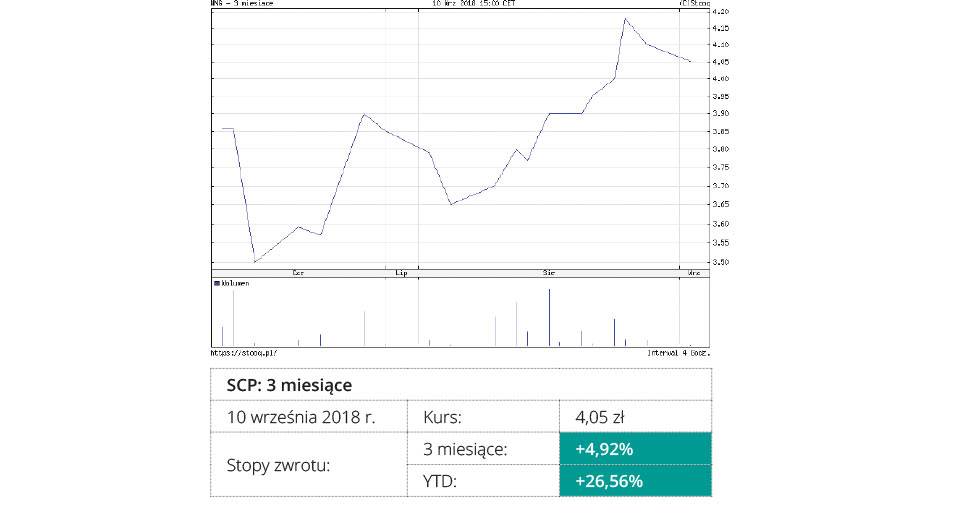
NanoVelos, spółka zależna NanoGroup, skupia się obecnie na rozwoju POLEPI, który jest najbardziej zaawansowanym projektem spółki i jednocześnie pierwszym kandydatem na nowy lek stworzony w ramach platformy Drug Delivery. To innowacyjne rozwiązanie polega na enkapsulowaniu (umieszczaniu) w nanocząstkach polisacharydowych epirubicyny, która jest powszechnie stosowanym cytostatykiem, znajdującym zastosowanie w leczeniu m.in. nowotworów piersi, jajnika czy jelita grubego. Epirubicyna od wielu lat jest bardzo szeroko stosowana w leczeniu wielu różnych nowotworów i często jest pierwszym wyborem przy rozpoczęciu leczenia onkologicznego.
Spółka jest obecnie w trakcie badań przedklinicznych i spodziewa się, że doprowadzi POLEPI do fazy badań klinicznych pod koniec 2019 r. Do tego momentu NanoVelos chce również pozyskać partnera, który pomoże jej doprowadzić badania do końca i skomercjalizować cały projekt. Celem spółki jest zakończenie badań klinicznych w 2021 r. ? wtedy też ma nastąpić komercjalizacja POLEPI.
Do tej pory badania nad POLEPI kosztowały ok. 1,8 mln zł. Spółka przewiduje, że przeprowadzenie pozostałych badań klinicznych i doprowadzenie projektu do fazy badań klinicznych będzie kosztować kolejne ok. 3,5 mln zł.
PBKM
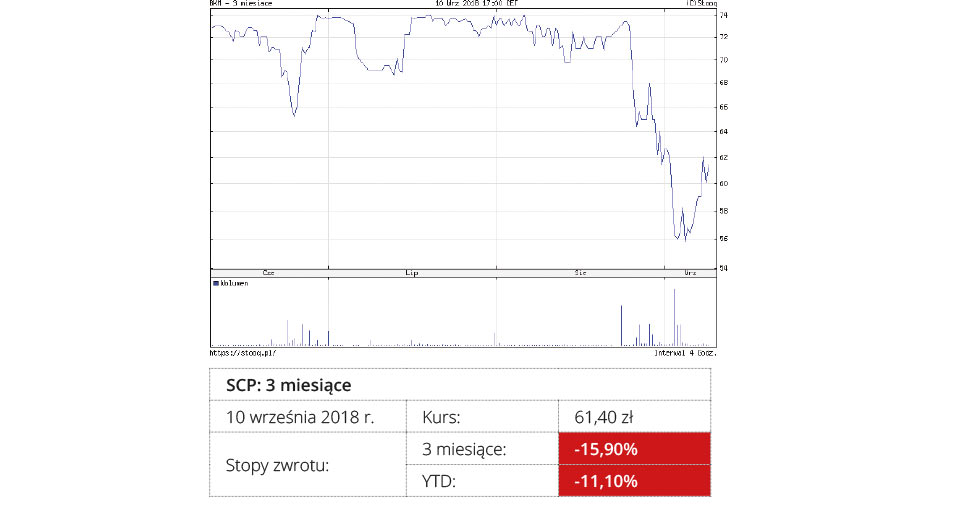
PBKM najbardziej skupia się opracowaniu produktu leczniczego terapii zaawansowanej opartej na komórkach mezenchymalnych z galarety Whartona w leczeniu stwardnienia zanikowego bocznego (ALS). Obecne metody terapii tej choroby nie oferują żadnego skutecznego leczenia. Potencjał rynku dla leku na stwardnienie zanikowe boczne, nad którym pracuje PBKM, szacowany jest na 1,7 mld dolarów amerykańskich.
Celem badań prowadzonych przez PBKM będzie wykazanie klinicznego bezpieczeństwa i skuteczności leczenia stwardnienia zanikowego bocznego przy użyciu komórek macierzystych oraz opracowanie panelu badań diagnostycznych, które pozwolą określić, którzy pacjenci mogą lepiej reagować na terapię komórkową.
Badania przedkliniczne rozpoczęły się w 2018 r. Łącznie badania kliniczne fazy II/III obejmą ponad 100 pacjentów. Ich zakończenie jest planowane za ok. 5 lat.
Projekt badań PBKM nad lekiem na ALS zdobył dofinansowanie z Narodowego Centrum Badań i Rozwoju (NCBiR) w ramach platformy INNO NEURO PHARM. Dofinansowanie obejmuje ok. 50 proc.nakładów na realizację badań, które w całości wyniosą ok. 24 mln zł.
Celon Pharma
Pipeline innowacyjny projekt Celon Pharmy obejmuje obecnie 12 leków innowacyjnych. Najbardziej zaawansowanym jest rozwój esketaminy w leczeniu depresji. Jest to substancja o dobrze znanym profilu bezpieczeństwa. Dotychczas była rozwijana głównie w obszarze anestezji. Warszawska Spółka rozwija ją w depresji lekoopornej, w podaniu inhalacyjnym, w wygodnym dla pacjentów inhalatorze suchego proszku. Obecnie Spółka rozpoczyna badanie kliniczne II fazy w całej Polsce.
Całkowity koszt projektu, obejmujący II fazę kliniczną, wynosi ponad 24 mln złotych, a kwota dofinansowania z NCBiR to ponad 12 mln zł. Spółka powinna być gotowa do złożenia wniosków rejestracyjnych w Europie i USA w 2022 r. III faza badań klinicznych powinna potrwać 3-3,5 roku. Koszt realizacji III fazy badania klinicznego Spółka szacuje na 40-50 mln euro. Celon Pharma chce zrealizować ją wraz z partnerem. Po odczytaniu wyników II fazy klinicznej, zarząd deklaruje, że będzie gotowy na sfinalizowanie umowy partneringowej. W połowie 2019 r. powinna być gotowa podpisać umowę.








