Dzięki specjalnemu mikroskopowi naukowcy poznali, jak rozwija się mysz. Komórka po komórce. Los każdej z nich, powstawanie tkanek i organów możemy teraz obejrzeć na kolorowej ruchomej i interaktywnej mapie. To podwaliny pod przyszłe transplantacje organów.
Kluczowe pytanie biologii brzmi: jak powstaje organizm? Na rozum, jeśli dla większości stworzeń wielokomórkowych, do których należymy także my, początkiem jest jedna komórka, zwana zygotą, to jak z niej powstają te miliardy różnorodnych i spełniających rozmaite funkcje, a w dodatku ściśle ze sobą współpracujących komórek?
Wyzwanie dla naukowców
Cud rozwoju ssaka jest jednym z kilku, które chcielibyśmy jak najdokładniej podpatrzeć. Na poziomie genetycznym ? jakie geny kiedy się włączają, a jakie wyłączają ? to doskonale już wiadomo. Na poziomie ogólnego oglądu też ? wszak współczesne kamery potrafią sfilmować bardzo dokładnie organizm dowolnego zwierzęcia w trakcie jego przemian rozwojowych. Jednak na samym początku zarodek jest maleńki, mikroskopijny, a dzieją się w nim rzeczy dla przyszłości danego zwierzęcia czy człowieka najistotniejsze. Prześledzenie zatem i dogłębne poznanie losu każdej z komórek ? skoro z jednej rozwinie się kiedyś skóra, a z innej mózg, z jeszcze innej mięsień sercowy ? jest od lat wyzwaniem dla naukowców i lekarzy.
Zauważmy też, że na początku te kilka komórek zarodka powstałych po tym, jak zygota podzieli się na dwie komórki, te z kolei dadzą cztery, a te następnie osiem, wydaje się całkowicie identyczne i zdolne do wszystkiego. Jeśli bowiem zygota podzieli się na dwie komórki potomne i taki zarodek się rozpadnie, to rodzą się bardzo do siebie podobne bliźnięta.
W biologii najczęściej próbujemy poddać obserwacji i analizie tzw. organizmy modelowe, pozwalające na wyciąganie wniosków w kwestii: a jak to jest u człowieka? Wśród najlepiej zbadanych modeli nie znajdziemy już dziś słynnego przed wiekiem laboratoryjnego królika. Na liście są raczej bakteria pałeczka okrężnicy, drożdż piekarski, maleńki wolno żyjący nicień Caenorhabditis elegans (genetyka rozwoju zaczęła swój rozkwit od badań tego ?robala?), muszka owocowa, rybka akwariowa danio pręgowany, no i mysz. Wszystkie modele muszą być tanie, szybko się rozwijać i dawać łatwo manipulować genetycznie.
Jak obejrzeć żywe zarodki?
Nowatorska technika mikroskopowa, zwana LSFM (ang. light sheet fluorescence microscopy), posłużyła 10 lat temu do przyjrzenia się zarodkowi muszki owocowej i danio pręgowanego. Ten ostatni, choć kręgowiec, to znacznie od człowieka odleglejszy ewolucyjnie niż mysz. No i o znacznie mniej skomplikowanym zarodku. Ssaki są tu naprawdę trudniejsze do podglądania i naukowcy potrzebowali całej dekady, by udoskonalić technikę mikroskopową oraz komputerową rejestrację i analizę uzyskiwanych obrazów, aby wreszcie zrobić wielkie podejście do rozwoju myszy.
LSFM omija pewien podstawowy problem mikroskopii: mikroskop widzi ostro tylko w jednym punkcie, czy też w jednej płaszczyźnie. Stąd np. dla klasycznego mikroskopu świetlnego, a także elektronowego, preparat nie może być za gruby. Im bardziej jest ultracienki, tym lepsza obserwacja. No ale żeby coś pokroić, trzeba to najpierw zabić i utrwalić. Tak potraktowany zarodek już w nic się nam nie rozwinie. To ograniczenie techniczne pozostaje w mocy także dla tzw. mikroskopu konfokalnego. Ten z kolei potrafi, niczym tomograf komputerowy, pokroić optycznie jakąś grubą, choć mikroskopijną rzecz na plasterki, i poddać obserwacji każdy z tych plasterków z osobna. Jednak wymaga to, by ta obserwowana rzecz też była najpierw utrwalona, a zatem martwa.
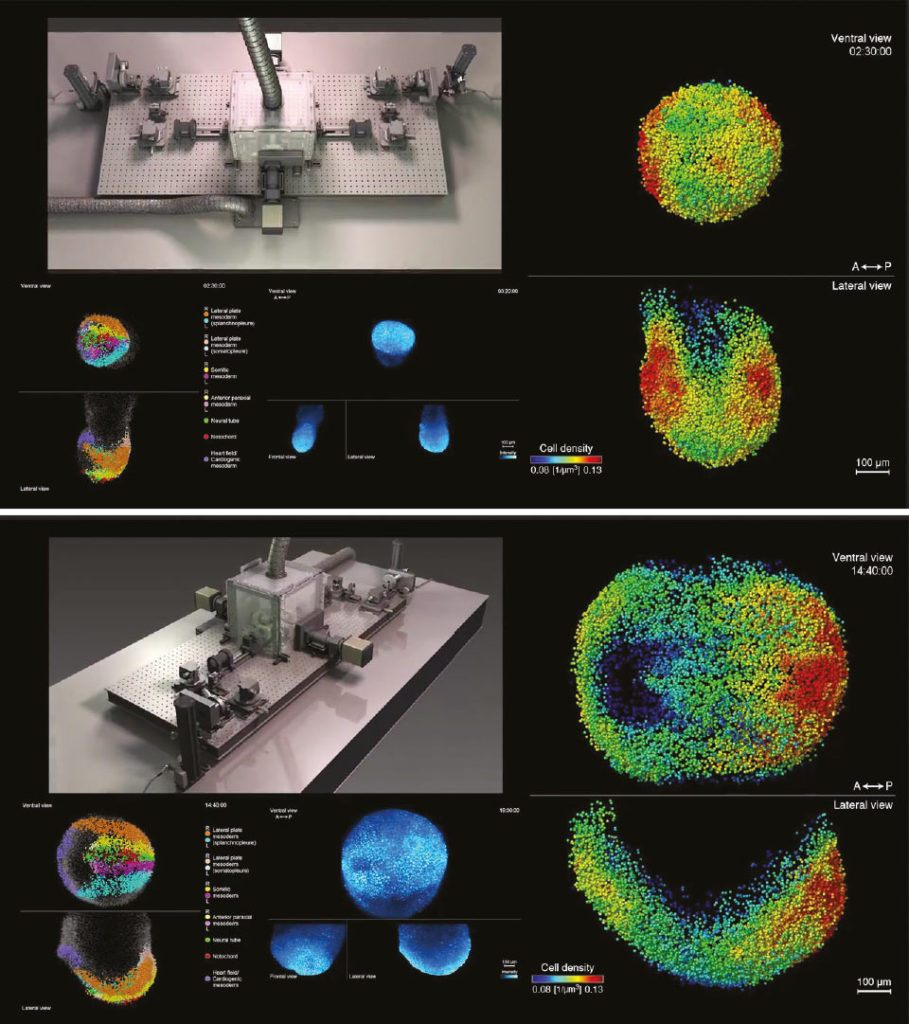
LSFM potrafi oglądać żywe zarodki. I widzieć je ostro. Aby jednak poradzić sobie z myszą od momentu, gdy jej zarodek zagnieżdża się w macicy aż do powstawania w nim zawiązków organów, musiał zostać wyposażony w sztuczną inteligencję. Ona potrafiła sama uczyć się z gromadzonych danych. Było to niezbędne, bo zarodek, będąc żywym, nie tylko się rusza, czy też ulega ruchom płynów, w których jest zawieszony, ale i nieustannie rośnie. Np. o rząd wielkości przez 2 dni. Czyli, gdybyśmy w dniu 6. obserwowali coś o grubości 1 mm, to dwa dni później mamy już do czynienia z obiektem o grubości 1 cm!
Komórka po komórce
Specjalne algorytmy komputerowe były też niezbędne do sortowania milionów uzyskanych zdjęć tak, by śledzić każdą pojedynczą komórkę z osobna podczas jej podziałów i ruchów ? bo komórki podczas rozwoju lubią się przemieszczać! Wgłębiają się, zapadają pod inne, wędrują na drugi koniec zarodka itp. W trakcie wczesnego rozwoju komórki ze sobą współdziałają i jedne wpływają na drugie. Komórki podczas swego wzrostu i rozwoju zmieniają również wiele parametrów fizyko-chemicznych. A to powoduje zmiany własności optycznych. Nie są one cały czas np. tak samo transparentne, nie w taki sam sposób odbijają światło. Dla mikroskopu to wyzwanie, by cały czas tak się regulować, aby to wszystko niwelować.
Aby stworzyć wiarygodny i pełny obraz, czy raczej film, oraz interaktywną dynamiczną mapę rozwoju zarodkowego myszy, naukowcy wykorzystali kilka niezależnych eksperymentów, czyli kilka zarodków. Dziś efekt ich trudnej pracy jest dostępny za darmo przez internet dla tysięcy embriologów i medyków na całym świecie. Można się z nim zapoznać na łamach najbardziej prestiżowego czasopisma w zakresie biologii, ?Cell?. Zanim powstaną metody uzyskiwania w laboratorium narządów ludzkich do transplantacji, musimy wiedzieć, jak te organy rozwijają się naturalnie. Komórka po komórce. I po to prowadzi się takie badania.
Post scriptum: Opisane powyżej naukowe przedsięwzięcie zakończone sukcesem wygrało ranking tygodnika ?Science? na ?Przełom naukowy roku 2018?. Można z samym owym rankingiem zapoznać się tu: https://vis.sciencemag.org/breakthrough2018/?utm_source=newsletters&utm_medium=newsletter&utm_campaign=468×60-22502&et_rid=379130090&et_cid=2573556.