Keratoplastyka selektywna endotelialna
Do niedawna zdecydowaną większość zabiegów naprawczych rogówki za pomocą przeszczepienia stanowiły przeszczepienia drążące, czyli takie, w których wymieniana jest pełna jej grubość. Od kilku lat zarówno na świecie, jak i w Polsce obserwuje się stały wzrost odsetka przeszczepień selektywnych, szczególnie keratoplastyki endotelialnej (selektywna wymiana śródbłonka ? najbardziej wewnętrznej warstwy rogówki, od której zależy odpowiedni stopień uwodnienia całej tkanki, jej grubość i przezierność optyczna). Według raportu amerykańskiego banku tkanek oka z 2017 roku, liczba przeszczepień drążących wyniosła 18 346 (spadek o 1,3 proc.), podczas gdy liczba przeszczepów endotelialnych wzrosła o 2,6 proc., czyli do 28 993 zabiegów[1]. W Polsce w skali roku liczby te są nieosiągalne, przede wszystkim z powodu zbyt małej dostępności tkanek w stosunku do potrzeb (ten problem nie występuje w USA i wielu innych krajach). W 2017 roku w Polsce wykonano łącznie 1298 przeszczepień rogówki[2].
Podobne do światowych i amerykańskich tendencje wzrostu odsetka przeszczepień śródbłonkowych obserwuje się także w Polsce. W Samodzielnym Publicznym Klinicznym Szpitalu Okulistycznym w Warszawie liczba zabiegów keratoplastyki warstwowej tylnej rośnie z każdym rokiem. Ograniczeniem realizacji tej formy terapii chorób rogówki jest niewystarczająca dostępność odpowiedniego materiału do przeprowadzenia operacji. Na aktualnej liście pacjentów oczekujących na przeszczepienie rogówki w naszym ośrodku około 52 proc. biorców jest zakwalifikowanych do przeszczepu endotelialnego, a do drążącego 37 proc. Proporcje te wskazują, z jakimi rodzajami patologii rogówki, wymagającymi leczenia chirurgicznego, mamy obecnie do czynienia w praktyce klinicznej.
W miarę doskonalenia technik chirurgicznych oraz obserwowanych korzyści dla pacjenta, wynikających ze specyfiki procedur keratoplastyki selektywnej endotelialnej, wskazania do tego rodzaju zabiegu uległy rozszerzeniu. O dotychczasowych wskazaniach, zaletach i dokładnej technice zabiegu pisałam uprzednio w artykule pt. ?Przeszczepy warstwowe rogówki? w nr 4/2015 niniejszego czasopisma[3].
Choroby, w których dochodzi do upośledzenia funkcjonowania komórek śródbłonka i w konsekwencji dekompensacji całej rogówki (utraty jej przezierności, a w zaawansowanych stadiach ? rozwoju keratopatii pęcherzowej ze znacznym spadkiem ostrości wzroku i dolegliwościami bólowymi), to:
? dystrofia śródbłonkowa Fuchsa (FECD),
? pierwotna niewydolność komórek śródbłonka (bez FECD),
? dystrofia polimorficzna tylna (PPD) i inne rzadsze dystrofie śródbłonka,
? zespół śródbłonkowy tęczówkowo-rogówkowy (ICE),
? jatrogenne uszkodzenie śródbłonka (np. powikłanie operacji zaćmy) ? keratopatia obrzękowa w pseudosoczewkowości lub afakii (bezsoczewkowości),
? wtórna niewydolność śródbłonka w innych chorobach oczu, np. jaskrze, po zapaleniach rogówki (endothelitis) i przedniego odcinka błony naczyniowej,
? dekompensacja przeszczepienia drążącego niezależnie od reakcji immunologicznych lub po przebytej chorobie przeszczepu.
Idealnym kandydatem do przeszczepienia warstwowego tylnego jest pacjent z chorym śródbłonkiem i objawami keratopatii, bez zmian trwałych w pozostałych częściach rogówki, takich jak włóknienie i bliznowacenie. Jednak często nawet w zaawansowanej chorobie z początkowym włóknieniem decydujemy się na ten rodzaj przeszczepienia. Mimo iż po selektywnej wymianie tylnej części rogówki (endotelium), w przedniej warstwie rogówki własnej biorcy pozostają przymglenia (podnabłonkowe lub miąższowe), to pacjent znacznie szybciej wraca do funkcjonowania w życiu codziennym, niż po przeszczepieniu drążącym. Jest to związane z szybszym gojeniem, poprawą ostrości wzroku, brakiem szwów indukujących astygmatyzm pooperacyjny i dyskomfort czuciowy, stosunkowo mniejszym ryzykiem odrzutu i koniecznością procedur, takich np. procedur jak usuwanie szwów.
Obecnie najczęściej wykonuje się przeszczepienie endotelialne metodą DSAEK (ang. Descemet?s stripping automated endothelial keratoplasty), w którym u biorcy, po usunięciu chorej błony Descemeta (tzw. descemetoreksja), wszczepia się płatek dawcy przygotowany z użyciem mikrokeratomu. Płatek ten zawiera błonę Descemeta z bardzo dobrą gęstością zdrowych komórek śródbłonka oraz cześć miąższu rogówki o różnej grubości. W celu osiągnięcia bardzo cienkiego płatka dawcy można posłużyć się modyfikacją UT-DSAEK (ang. Utra-thin Descemet?s stripping automated endothelial keratoplasty), w której ultracienki płatek dawcy preparowany jest przez dwukrotne cięcia mikrokeratomem.
W krajach, w których dostępność tkanek do przeszczepień rogówki jest wystarczająca, obserwuje się tendencję rosnącą liczby zabiegów metodą DMEK (ang. Descemet?s membrane endothelial keratoplasty) ? czyli przeszczepienia samej błony Descemeta z komórkami śródbłonka.
DSAEK jest metodą preferowaną w skomplikowanych oczach
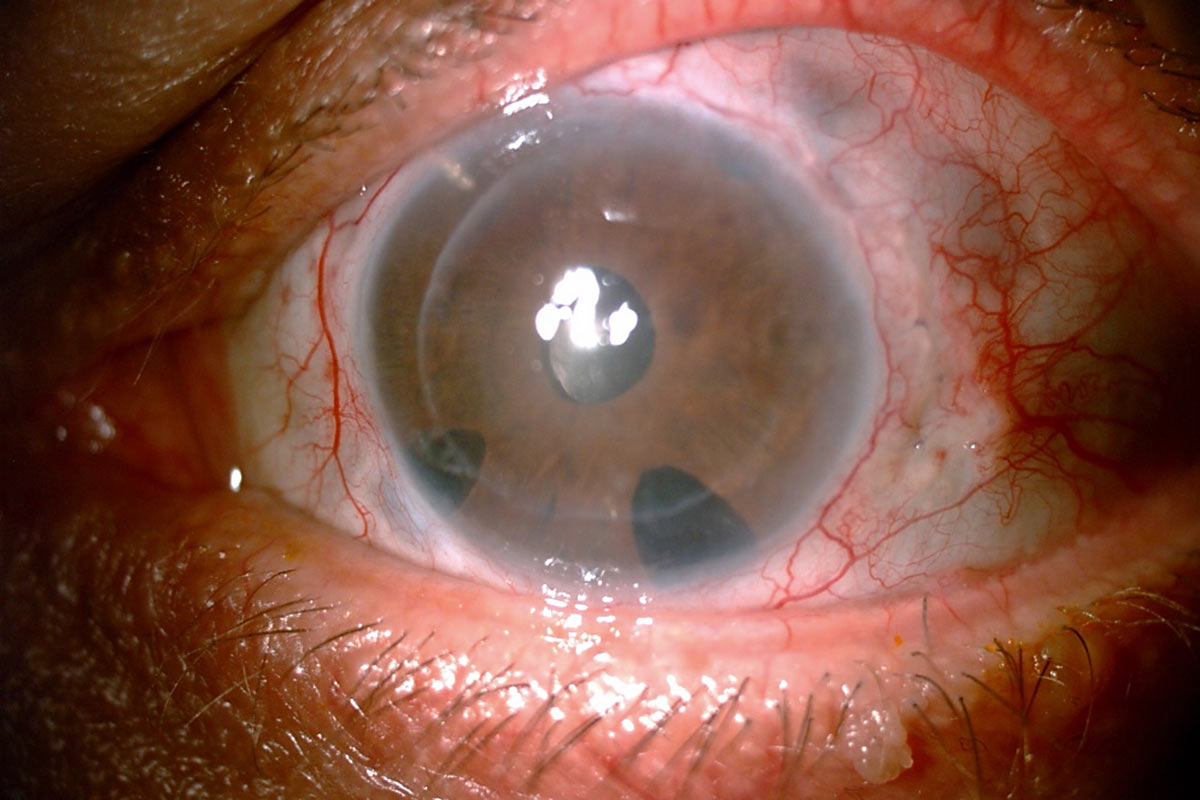
Obecnie z przeszczepienia metodą DSAEK nie dyskwalifikuje pacjenta, jak miało to kiedyś miejsce, obecność w oku nietypowych implantów soczewkowych, przebyta chirurgia jaskry z obecnością minisetonów Express (Fot.1) czy zastawki Ahmeda (Fot. 2a-b). W tych przypadkach istnieje oczywiście wyższe ryzyko śród- i pooperacyjnego uszkodzenia płatka przeszczepu, ale korzyści po wprawnie przeprowadzonej keratoplastyce endotelialnej w porównaniu z przeszczepieniami drążącymi są warte jego podjęcia. Wieloletnie doświadczenie chirurgiczne pozwala na efektywne przeprowadzenie zabiegu nawet w bardzo skomplikowanych oczach.
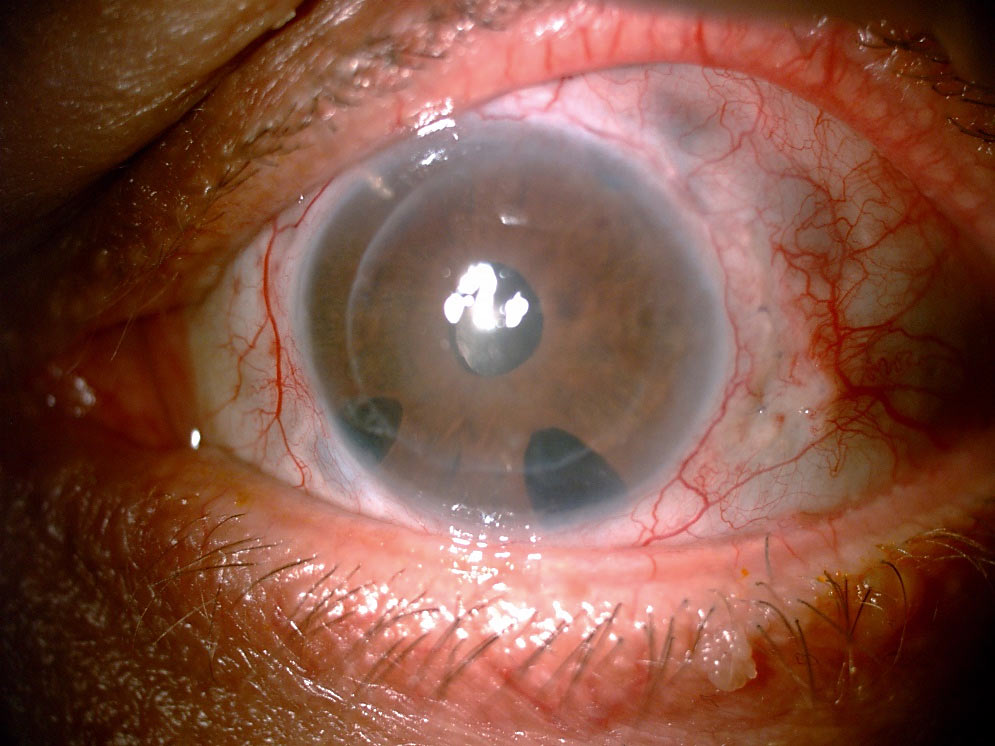
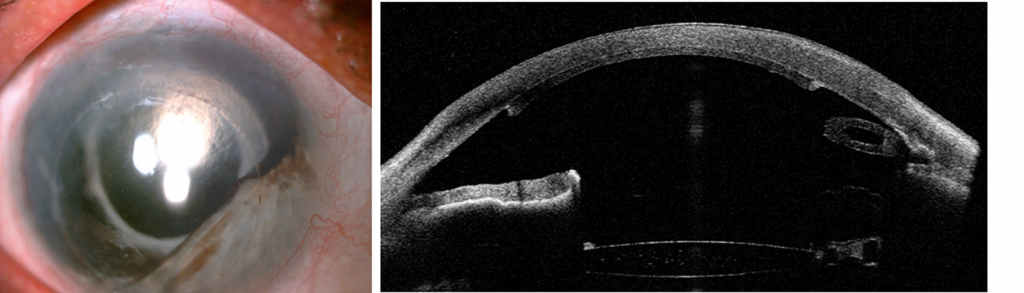
pseudofakią, a) widok z lampy szsczelinowej, b) przekrój horyzontalny w badaniu AS-OCT
DSAEK, a nie DMEK, jest metodą z wyboru w przypadkach: obecności implantu soczewki w przedniej komorze (ACIOL), braku soczewki (afakii), dużych irydektomii (ubytku tęczówki po jej wycięciu), sektorowego braku tęczówki (aniridii), zrostach rogówkowo-tęczówkowych, w oczach po witrektomii (wycięciu ciała szklistego), obecności szwów na tęczówce (po jej plastyce) i implantów fiksowanych szwami, obecności w komorze przedniej rurki implantów drenujących w oczach z jaskrą, w oczach po uprzedniej keratoplastyce drążącej i dekompensacji przeszczepu. W sytuacjach zaawansowanych zmian utrudniających wgląd do komory przedniej oka również preferowaną metodą jest DSAEK, w której łatwiejsze jest odpowiednie ułożenie płatka bez dobrej widoczności[4]. W takich zabiegach pomocne jest śródoperacyjne badanie optycznej koherentnej tomografii OCT struktur przedniego odcinka gałki ocznej, jednak jest ono możliwe w niewielu ośrodkach. U pacjentów, u których wiodącą przyczyną zabiegu nie jest poprawa widzenia, ale np. zniwelowanie dolegliwości bólowych (w keratopatii pęcherzowej w oku słabo rokującym), należy wykonać DSAEK, a nie DMEK.
Retransplantacje
Ponowna transplantacja rogówki w przypadku dekompensacji pierwotnego przeszczepu ma zawsze gorsze rokowanie. Do niedawna obowiązywała zasada wykonania retransplantacji taką samą techniką lub keratoplastyki drążącej po zdekompensowanym przeszczepieniu warstwowym. W rzadkich przypadkach nieudanych przeszczepień endotelialnych ponowne przeszczepienie polega na wymianie płatka na nowy. W częściej występujących dekompensacjach przeszczepień drążących do tej pory wykonywano keratoplastykę drążącą o wielkości takiej samej lub większej średnicy nowego płatka przyszywanego szwami. Obecnie z powodzeniem coraz częściej korzystamy z techniki wymiany selektywnej endotelium (Fot. 3a-b), bo spadek gęstości śródbłonka (w różnych mechanizmach) jest główną przyczyną utraty funkcji pierwotnego przeszczepu. Taki rodzaj retransplantacji jest korzystniejszy dla pacjenta, ponieważ znacznie skraca okres rekonwalescencji i eliminuje wady związane z dużym śródoperacyjnym otwarciem gałki ocznej, pełnościenną raną pooperacyjną i obecnością licznych szwów, oraz reakcją immunologiczną odrzutu pochodzenia nabłonkowego i miąższowego[5].
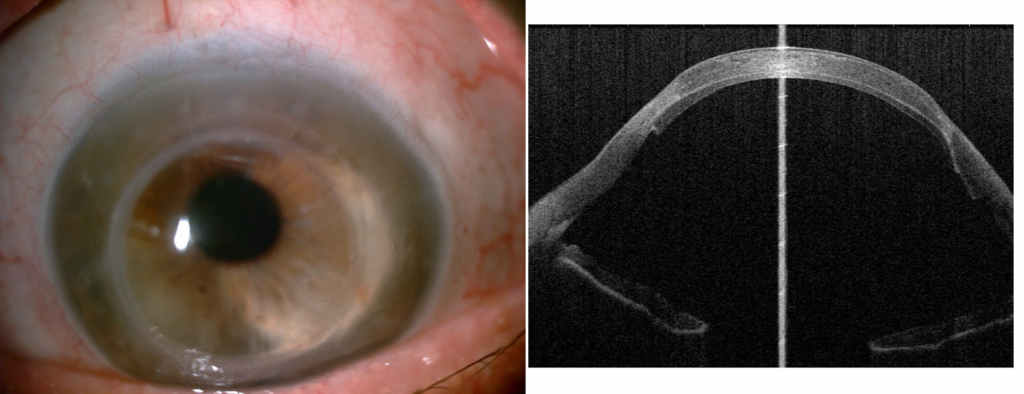
dekompensacji pierwszego przeszczepu: a) widok w lampie szczelinowej; b) obraz w badaniu AS-OCT
Operację przeszczepienia rogówki można rozszerzyć o dodatkowe procedury: usunięcie zaćmy z wszczepem lub bez wszczepu sztucznej soczewki (najczęstsza procedura to facoDSAEK, czyli usunięcie zaćmy metodą fakoemulsyfikacji z wszczepieniem sztucznej soczewki i przeszczepieniem endotelialnym), wszczep wtórny implantu (fiksowanego do tęczówki lub śródtwardówkowo), usunięcie zrostów, wykonanie plastyki tęczówki.
Doniesienia o rozwoju innych metod w terapii uszkodzeń endotelium rogówki dotyczą głównie najczęstszej przyczyny, czyli dystrofii Fuchsa. W chorobie tej najbardziej zmieniony jest obszar centralny, natomiast na obwodzie często obecne są zdrowe komórki, które w odpowiednich warunkach mogą przemieszczać się, wypełniając luki. Znaną i stosowaną czasem procedurą jest descemetoreksja (usunięcie chorej błony Descemeta pacjenta) bez przeszczepienia allogenicznego płatka, po której obserwuje się zmniejszenie obrzęku i poprawę przezierności rogówki w czasie około 3-6 miesięcy[6,7]. Opisany został przypadek przeszczepienia bezkomórkowej błony Descemeta (pozbawionej śródbłonka) celem ułatwienia transferu komórek z obwodu[8]. Opublikowano doniesienia przeszczepiania fragmentów błony Descemeta jako wystarczające dla poprawy przezierności rogówki[9]. Na modelach zwierzęcych bada się skuteczność przeszczepień wyhodowanych komórek o właściwościach różnicowania się w endotelium rogówki[10,11]. W Japonii w nierandomizowanym badaniu wykonano iniekcje komórek ludzkiego endotelium z hodowli komórkowej u 11 pacjentów z zadowalającym efektem w dwuletnim okresie obserwacji[12].
O ile w chorobach endotelium przeszczepienia samych komórek są w fazie eksperymentu i nie są dostępne w codziennej praktyce klinicznej, to przeszczepienia autologiczne komórek macierzystych rąbka rogówki są już całkiem bliską perspektywą.
Przeszczepienia komórek macierzystych rąbka rogówki
Przeszczepienia rąbkowe dostarczają rąbkowych komórek macierzystych (RKM), niezbędnych dla utrzymania prawidłowej powierzchni rogówki. Są one nieodzowne dla funkcji narządu wzroku, a ich przeszczepianie stanowi szczególny rodzaj keratoplastyki. Leczenie operacyjne zmętniałych rogówek z powodu niewydolności RKM za pomocą przeszczepień drążących lub warstwowych zazwyczaj kończy się niepowodzeniem.
Niewydolność RKM może być pierwotna lub wtórna. Najczęstszą przyczyną tej ostatniej są oparzenia chemiczne lub termiczne oczu. Zmiany degeneracyjne rozwijają się przez wiele miesięcy od urazu i w zależności od stopnia destrukcji RKM objawiają się: ubytkami nabłonka, tworzeniem patologicznych naczyń w miejscach, które powinny być awaskularne, bliznowaceniem rogówki (bielmem), tworzeniem zrostów spojówki, zrostów powiekowo-gałkowych i malformacji powiek, formowaniem pseudoskrzydlika i łuszczki narastającej na rogówkę, odkładaniem się twardych złogów w nabłonku (keratopatia taśmowata), ale też rozmiękaniem rogówki, z powstaniem owrzodzeń, a nawet perforacji.
Obustronna ciężka niewydolność RKM równa się praktycznej ślepocie. Jedyną metodą przywrócenia widzenia jest wykonanie chociażby w jednym oku przeszczepienia rąbkowego, a w kolejnym etapie keratoplastyki optycznej (najczęściej drążącej). Od lat 90. wykonuje się przeszczepienia allogeniczne rąbków od dawców zmarłych, stosując techniki chirurgiczne wg Tsuboty[13] i Hollanda[14]. Ze względu na wysoką immunogenność płatków rogówkowo-twardówkowych niezbędne jest stosowanie wielomiesięcznej immunosupresji ogólnej, która obarczona jest działaniami niepożądanymi. Dlatego w przypadkach jednostronnej niewydolności RKM poszukuje się innych metod, w których można byłoby wykorzystać autologiczne komórki rąbka ze zdrowszego oka pacjenta. Teoretycznie nośnikami RKM mogą być: spojówka, błona owodniowa, podłoża fibrynowe i inne wytworzone w procesach bioinżynierii (np. poliuretan, polikaprolakton), ale dostarczone komórki muszą przetrwać transfer i podjąć funkcje w miejscu docelowym. Osiągnięcie tego okazuje się w praktyce bardzo trudne. Rozwiązaniem mogą być hodowle komórkowe, prowadzone w specjalnych, standaryzowanych warunkach laboratoryjnych ze ścisłą kontrolą procesu namnażania, różnicowania i przeżywalności komórek.
Samodzielny Publiczny Kliniczny Szpital Okulistyczny w Warszawie jest jednym z dwóch ośrodków w Polsce, w których prowadzone jest międzynarodowe wieloośrodkowe badanie kliniczne, oceniające skuteczność i bezpieczeństwo przeszczepienia hodowli tkankowej autologicznych komórek rąbka rogówki w odtworzeniu nabłonka rogówki u pacjentów z niewydolnością RKM spowodowaną oparzeniami oka (Holocore, Chiesi Farmaceutici S.p.A.). Do badania kwalifikowani są pacjenci z umiarkowanym lub ciężkim niedoborem RKM, po minimum dwóch latach od oparzenia. Z oka zdrowszego pobiera się niewielki bioptat rąbka rogówki ? ok. 2mm2. To bardzo mało w porównaniu z procedurą autologicznego przeszczepu spojówkowo-rąbkowego (ang. conjuctival limbal autograft, CLAU), w którym pobiera się bioptat wielkości 20 mm2. Bioptat rąbka wysyłany jest przy zachowaniu określonych warunków do laboratorium we Włoszech, gdzie na odpowiednim nośniku fibrynowym hoduje się zdrowe komórki do uzyskania 79 000-316 000 komórek/cm2, z czego średnio 3,5% stanowią komórki macierzyste (produkt leczniczy o nazwie Holoclar). Holoclar jest implantowany do chorego oka pacjenta po około 6 miesiącach od biopsji. Dotychczasowe doniesienia z ośrodków uczestniczących w badaniu na temat efektywności leczenia są bardzo pozytywne.15.
Postęp w terapii chorób rogówki dzieje się na naszych oczach. Dotyczy on zarówno technik chirurgicznych, pozyskiwania i hodowania potrzebnych komórek i tkanek, ale także prób zastosowania terapii genowej. Intensywne badania z zakresu biologii molekularnej w dystrofiach rogówki, np. dystrofii Fuchsa, są obecnie prowadzone przez genetyków we współpracy z lekarzami z Samodzielnego Publicznego Klinicznego Szpitala Okulistycznego w Warszawie.
tekst:
dr n. med. Monika Udziela | Prof. dr hab. n. med. Jerzy Szaflik | Prof. dr hab. n. med. Jacek P. Szaflik | Katedra i Klinika Okulistyki II WYDZIAŁU Lekarskiego Warszawskiego Uniwersytetu Medycznego | Samodzielny Publiczny Kliniczny Szpital Okulistyczny w Warszawie
Piśmiennictwo:
1. 2017 Eye Banking Statistical Report, Eye Bank Association of America
2. Dane z rejestru przeszczepień Poltransplantu
3. Szaflik J.P., Izdebska I., Udziela M. ?Przeszczepy warstwowe rogówki?. Świat Lekarza 4/2015 (40): 16-21.
4. Ophthalmology news – January 2018 COVER FEATURE All you need to know about cornea transplants New trends in endothelial keratoplasty by Rich Daly EyeWorld Contributing Writer. ASCRS Publication. EyeWorld20.
5. Ang M, Ho H, Wong C, Htoon HM, Meh.ta JS, Tan D. Endothelial keratoplasty after failed penetrating keratoplasty: an alternative to repeat penetrating keratoplasty. Am J Ophthalmol. 2014;158(6):1221-7.
6. Van den Bogerd B., Dhubhghaill S.N., Koppen .C, Tassignon M.J., Zakaria N. ?A review of the evidence for in vivo corneal endothelial regeneration?. Surv Ophthalmol. 2018 Mar – Apr;63(2):149-165.
7. Davies E., Jurkunas U., Pineda R. ?Predictive Factors for Corneal Clearance After Descemetorhexis Without Endothelial Keratoplasty?. Cornea. 2018 Feb;37(2):137-140.
8. Soh Y.Q., Mehta J.S. ?Regenerative Therapy for Fuchs Endothelial Corneal Dystrophy?. Cornea 2018, Apr;37(4): 523-7.
9. Zygoura V., Baydoun L., Ham L., Bourgonje V.J.A., van Dijk K., Lie J.T., Dapena I., Oellerich S., Melles G.R.J. ?Quarter-Descemet membrane endothelial keratoplasty (Quarter-DMEK) for Fuchs endothelial corneal dystrophy: 6 months clinical outcome?. Br J Ophthalmol. 2018 Jan 17.
10. Sun P., Shen L., Zhang C., Du L., Wu X. ?Promoting the expansion and function of human corneal endothelial cells with an orbital adipose-derived stem cell-conditioned medium?. Stem Cell Res Ther. 2017 Dec 20;8(1):287.
11. Okumura N., Matsumoto D., Fukui Y., Teramoto M., Imai H., Kurosawa T., Shimada T., Kruse F., Schlötzer-Schrehardt U., Kinoshita S., Koizumi N. ?Feasibility of cell-based therapy combined with descemetorhexis for treating Fuchs endothelial corneal dystrophy in rabbit model?. PLoS One. 2018 Jan 16;13(1):e0191306.
12. Schallhorn J.M. ?Novel treatment restores corneal clarity in patients with bullous keratopathy?. AAO. APR17, 2018.
13. Tsubota K., Toda I., Saito H., Shinozaki N., Shimazaki J. ?Reconstruction of the corneal epithelium by limbal allograft transplantation for severe ocular surface disorders?. Ophthalmology. 1995 Oct;102(10):1486-96.
14. Holland E.J. ?Epithelial transplantation for the management of severe ocular surface disease?. Trans Am Ophthalmol Soc. 1996;94:677-743.
15. www.ema.europa.eu