Operacja zaćmy to jedna z częściej przeprowadzanych procedur chirurgicznych. Dzięki nowoczesnym metodom często udaje się przywrócić pacjentom wzrok.
Aby efekt końcowy był w pełni osiągnięty, potrzebne są właściwie przeprowadzona procedura chirurgiczna bez powikłań i odpowiednie działanie pooperacyjne polegające w głównej mierze na opanowaniu procesów zapalnych wywołanych przez uraz chirurgiczny. W tym celu stosuje się leki o działaniu przeciwzapalnym w postaci steroidów i niesteroidowych leków przeciwzapalnych.
Zaćma według Światowej Organizacji Zdrowia (WHO, World Health Organization) to najczęstsza przyczyna ślepoty na świecie. Na szczęście stanowi ona odwracalną przyczynę. Operacja zaćmy jest jedną z częściej wykonywanych procedur chirurgicznych w krajach rozwiniętych. Dzięki rozwojowi metod operacyjnych w chirurgii soczewki możliwe jest uzyskanie efektu zadowalającego chirurga i pacjenta w postaci pełnej ostrości wzroku po zabiegu. W tym dobrym efekcie końcowym istotną rolę odgrywa zarówno samo przeprowadzenie procedury, jak i postępowanie pooperacyjne w postaci przyjmowania odpowiednich kropli do oczu przez pacjenta oraz odbywanie wizyt kontrolnych.
Postępowanie pooperacyjne
Polskie Towarzystwo Okulistyczne w 2014 roku wydało wytyczne dotyczące postępowania okołooperacyjnego w chirurgii zaćmy. Obejmują one przyjmowanie przez pacjentów kropli z antybiotykiem (z grupy fluorochinolonów) przez 7-14 dni po operacji oraz leków o działaniu przeciwzapalnym ? niesteroidowych leków przeciwzapalnych (NLPZ) przez okres co najmniej 4 tygodni oraz kortykosteroidu przez okres 2-4 tygodni. Rozważyć można również podanie mydriatyku o krótkim okresie działania przez okres kilku dni po zabiegu[1].
Działanie przeciwzapalne po operacji zaćmy
Operacja zaćmy, jak każda procedura chirurgiczna, wyzwala kaskadę reakcji zapalnych, stąd istotne jest odpowiednie leczenie, gdyż niekontrolowane zapalenie może prowadzić do zrostów tylnych, zapalenia błony naczyniowej lub wtórnej jaskry[2]. Obecnie w postępowaniu pooperacyjnym stosuje się dwa rodzaje leków, aby kontrolować zapalenie: niesteroidowe leki przeciwzapalne i steroidy. W celu ograniczenia stanu zapalnego oka najczęściej podaje się leki miejscowo w postaci kropli i maści, gdyż osiągają wysokie stężenie w tkankach oka, nie powodując jednocześnie działań niepożądanych związanych z preparatami podawanymi ogólnie.
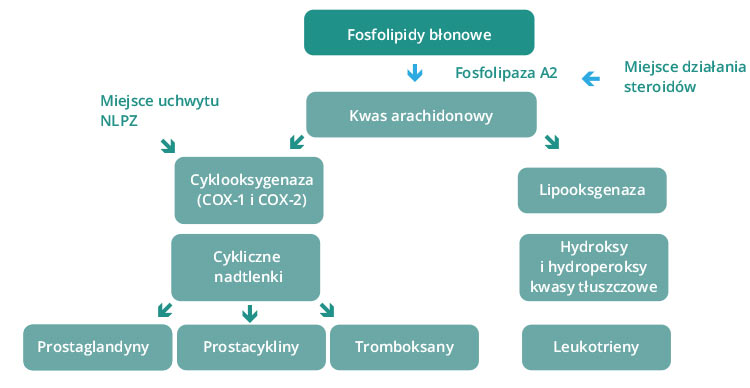
Zapalenie jest istotną reakcją obronną organizmu wywołaną przez uraz, który może być spowodowany przez czynniki fizyczne i chemiczne, drobnoustroje czy niedokrwienie. Angażuje ono mechanizmy immunologiczne, aby usunąć obcy materiał i uszkodzoną tkankę. W tych procesach pośredniczą chemiczne mediatory, takie jak prostaglandyny, tromboksan, leukotrieny[3]. Związki te pochodzą z przemian kwasu arachidonowego, który poprzez działanie fosfolipazy A2 jest uwalniany z fosfolipidów błonowych. Po dalszych przemianach w szlaku cyklooksygenaz powstają prostaglandyny i tromboksany, a po przejściu przez szlak lipooksygenaz powstają eikozanoidy. Oczne działanie prostaglandyn przejawia się w trzech aspektach[4]. Po pierwsze wpływają na ciśnienie wewnątrzgałkowe. W zależności od rodzaju uwolnionych prostaglandyn powodują jego podwyższenie lub obniżenie. Po drugie, działając na mięsień gładki tęczówki, wywołują zwężenie źrenicy. Oraz, po trzecie, zwiększają akumulację białek w cieczy wodnistej komory przedniej poprzez rozszerzenie naczyń i zwiększoną ich przepuszczalność. Kliniczne objawy produkcji prostaglandyn obejmują przekrwienie, zwężenie źrenicy, upośledzoną ostrość wzroku i ból. Steroidy i niesteroidowe leki przeciwzapalne wpływają na zmniejszenie produkcji prostaglandyn. Ich działanie różni się, ponieważ hamują kaskadę kwasu arachidonowego na różnych poziomach. Kortykosteroidy ograniczają rozwój odpowiedzi zapalnej poprzez blokadę enzymu fosfolipazy A2 odpowiedzialnego za powstawanie kwasu arachidonowego, a więc zmniejszają produkcję wszystkich jego pochodnych: prostaglandyn, tromboksanów i eikozanoidów. Przeciwzapalne działanie NLPZ z kolei ma związek z hamowaniem enzymów cykooksygenaz odpowiedzialnych za przemianę kwasu arachidonowego w prostaglandyny i tromboksany. Cyklooksygenaza występuje w postaci dwóch izoform: COX-1 i COX-2. COX-1 jest obecna w wielu komórkach i tkankach (np. w błonie śluzowej żołądka, śródbłonku naczyń, nerkach, płytkach krwi), jej druga forma (COX-2) powstaje w odpowiedzi na zapalenie czy uszkodzenie tkanek[5].
W obrębie okulistycznych preparatów steroidowych dostępne są: deksametazon, prednizolon, loteprednol i fluorometolon. Z niesteroidowych leków przeciwzapalnych możemy wybierać między diklofenakiem, ketorolakiem, nepafenakiem i bromfenakiem. NLPZ w obrębie swojej grupy różnią się między innymi siłą działania względem COX-1 i COX-2. Określa się to poprzez stężenie leku potrzebne do zahamowania działania enzymu cyklooksygenazy w 50% i wartość tę oznacza się symbolem IC50. Mniejsza wartość IC50 oznacza większą siłę hamowania enzymu. W badaniach in vitro dowiedziono, że bromfenak wykazuje się najsilniejszy potencjał do hamowania COX-2[6]. Wyróżnia się ponadto inną właściwością. Dodanie atomu bromu do cząsteczki zwiększyło jej lipofilność, dając lepszą penetrację tkankową[7-10]. W badaniach na zwierzętach dowiedziono, że bromfenak po miejscowym podaniu bardzo szybko osiąga mierzalne stężenie we wszystkich strukturach oka oraz jest wykrywany po 24 godzinach od miejscowego podania[11]. Dzięki tym właściwościom dobrej farmakokinetyki preparat może być stosowany tylko dwa razy dziennie. Poprawia to zdecydowanie stosowanie się pacjentów do zaleceń, czyli tak zwany compliance[12]. A to zapewnia szybką redukcję pooperacyjnego odczynu zapalnego i bólu.
Niesteroidowe leki przeciwzapalne znajdują zastosowanie w chirurgii okulistycznej z uwagi na profilaktykę zwężenia źrenicy podczas operacji zaćmy, opanowanie reakcji zapalnej po zabiegu oraz redukcję bólu i dyskomfortu po operacji zaćmy i zabiegach chirurgii refrakcyjnej, a także jako profilaktyka i leczenie torbielowatego obrzęku plamki po operacji zaćmy[13,14,15].
Wiele badań starało się porównać skuteczność działania przeciwzapalnego steroidów i NLPZ, aby ocenić, czy oba preparaty są niezbędne do opanowania odczynu zapalnego po operacji oraz czy ich działanie jest podobne lub uzupełniające się. Jedna z prac oparta na metaanalizie artykułów wykazała, że steroidy o umiarkowanym do silnego działaniu (betametazon, deksametazon, loteprednol i prednizolon) nie różniły się w sile działania przeciwzapalnego od niesteroidowych leków przeciwzapalnych. Słabsze steroidy, takie jak fluorometolon, działały ze zdecydowanie mniejszą siłą[2]. Przewagą NLPZ jest brak działań niepożądanych związanych ze stosowaniem steroidów, takich jak wzrost ciśnienia wewnątrzgałkowego i przyspieszenie powstawania zaćmy podtorebkowej tylnej, oraz mniejsze ryzyko infekcji wtórnych, szczególnie wirusowych.
Jedną z najczęstszych przyczyn pogorszenia widzenia po operacji zaćmy jest torbielowaty obrzęk plamki (CME, Cystoid Macular Edema), określany także jako zespół Irvine’a-Gassa. Jest to obrzęk siatkówki w plamce spowodowany akumulacją płynu[2]. Częstość jego występowania jest bardzo zróżnicowana. Klinicznie istotny CME związany z udokumentowanym pogorszeniem widzenia waha się od 0% do 4%[16,17,18]. CME rozpoznany poprzez obraz w angiografii fluoresceinowej dotyczy 9-30% pacjentów[16,17,19]. CME zdiagnozowany poprzez OCT jest odnotowany u 11-41% pacjentów [16,20,21,22]. Pacjenci, u których istnieje podwyższone ryzyko tego stanu, to osoby starsze, z cukrzycą, po panfotokoagulacji siatkówki, ze zwyrodnieniem barwnikowym siatkówki. Ryzyko zwiększają również stosowanie ogólnie lub miejscowo epinefryny, wcześniejsza operacja oczna. Śródoperacyjne czynniki ryzyka CME to przerwanie torby tylnej, zastosowanie soczewki fiksacyjnej i upływ ciała szklistego[5]. W przeprowadzonych badaniach udowodniono, że NLPZ w monoterapii i w terapii łączonej ze steroidami wykazują się większą skutecznością w zapobieganiu CME niż steroidy stosowane samodzielnie[23]. Potwierdza to metaanaliza 15 randomizowanych badań klinicznych (Kessel 2014). Wnioski płynące z tej metaanlizy to lepsza kontrola stanu zapalnego przez NLPZ niż steroidy i wyższa skuteczność w zapobieganiu CME[2].
Podsumowanie
Na pełen sukces operacji zaćmy wpływają właściwie przeprowadzona procedura i postępowanie pooperacyjne mające na celu przede wszystkim ograniczenie stanu zapalnego. W tym celu stosuje się steroidy i niesteroidowe leki przeciwzapalne. Obie grupy leków różnią się mechanizmem działania. Przez lata to steroidy były podstawową grupą leków stosowanych po operacji zaćmy. Zauważono, że dodanie leku z grupy NLPZ ogranicza częstość występowania torbielowatego obrzęku plamki oraz że w wielu przypadkach ich siła działania przeciwzapalnego jest porównywalna ze steroidami. Obecnie rekomenduje się łączenie tych preparatów po operacji zaćmy ze względu na ich addytywny charakter działania w zakresie ograniczania procesów zapalnych.
Piśmiennictwo:
1. Jurowski P., Kęcik D., Omulecki W., Romaniuk W., Szafilk J., Szaflik J.P. ?Postępowanie okołooperacyjne w chirurgii zaćmy?. Wytyczne Polskiego Towarzystwa Okulistycznego. 2014.
2. Kessel L., Tendal B., J?rgensen K.J., Erngaard D., Flesner P., Andresen J.L., Hjortdal J. ?Post-cataract prevention of inflammation and macular edema by steroid and nonsteroidal anti-inflammatory eye drops: a systematic review?. Ophthalmology 2014, Oct121(10);1915-1924.
3. Harry J., Mission G. ?Clinical Ophthalmic Pathology: Principles of Diseases of the Eye and Associated Structures?. Butterworth Heinemann, Oxford, UK, 2001.
4. Chang J.H., Chung H. ?Non-steroidal anti-inflammatory drug and endotoxin induced uveitis?. Korean. J. Ophthalmol. 7:35?42 (1993).
5. Langwińska-Wośko E., Bielecka A., Ambroziak A., Skopiński P. ?Niesteroidowe leki przeciwzapalne w okulistyce?. Kontaktologia i Optyka Okulistyczna, 2011;3:17-22.
6. Donnenfeld E., Donnenfeld A. ?Global Experience With Xibrom (Bromfenac Ophthalmic Solution) 0.09%: The First Twice-daily Ophthalmic Nonsteroidal Anti-inflammatory Drug?. Global Experience with Xibrox, 21-40.
7. Walsh D.A., Moran H.W., Shamblee D.A., et al. ?Antiinflammatory agents. 3. Synthesis and pharmacological evaluation of 2-amino-3-benzoylphenylaceticacid and analogues?. J Med Chem. 1984;27(11):1379?1388.
8. Sancilio L.F., Nolan J.C., Wagner L.E., Ward J.W. ?The analgesic and antiinflammatory activity and pharmacologic properties of bromfenac?. Arzneimittelforschung. 1987;37(5):513?519.
9. Ruiz J., López M., Mil? J., Lozoya E., Lozano J.J., Pouplana R. ?QSAR and conformational analysis of the anti-inflammatory agent amfenac and analogues?. J Comput Aided Mol Des. 1993;7(2):183?198.
10. Kida T., Kozai S., Takahashi H., Isaka M., Tokushige H., Sakamoto T. ?Pharmacokinetics and efficacy of topically applied nonsteroidal antiinflammatory drugs in retinochoroidal tissues in rabbits?. PLoS One. 2014;9:e96481.
11. Bakalyan G.A., Deshmukh H.M., Patterson H., et al. ?Concentrations of radioactivity in ocular tissues after a single topical dose of 14C-bromfenac ophthalmic solution. Proceedings of the American Society of Cataract & Refractive Surgery (ASCRS)?. Meeting, San Francisco, CA, March 17?22, 2006. Abstract P227.
12. Ikeda H., Sato M., Tsukamoto H., et al. ?Evaluation and multivariate statistical analysis of factors influencing patient adherence to ophthalmic solutions?. Yakugaku Zasshi. 2001;121:799?806.
13. O?Brien T.P. ?Emerging guidelines for the use of NSAID therapy to optimize cataract and patient care?. Curr Med Res Opin. 2005;21:1131?1137.
14. McColgin A.Z., Raizman M.B. ?Efficacy of topical Voltaren in reducing the incidence of postoperative cystoid macular edema?. Invest Ophthalmol Vis Sci. 1999;40:S289.
15. Heier J.S., Topping T.M., Baumann W. et al. ?Ketorolac versus prednisolone versus combination therapy in the treatment of acute pseudophakic cystoid macular edema?. Ophthalmol. 2000;107:2034?2038.
16. Guo S., Patel S., Baumrind K., et al. ?Management of pseudophakic cystoid macular edema?. Surv Ophthalmol. 2015;60(2):123?137.
17. Kim S.J., Bressler N.M. ?Optical coherence tomography and cataract surgery?. Curr Opin Ophthalmol. 2009;20(1):46?51.
18. Henderson B.A., Kim J.Y., Ament C.S., Ferrufino-Ponce Z.K., Grabowska A., Cremers S.L. ?Clinical pseudophakic cystoid macular edema: risk factors for development and duration after treatment?. J Cataract Refract Surg. 2007;33:1550?1558.
19. Mentes J., Erakgun T., Afrashi F., Kerci G. ?Incidence of cystoid macular edema after uncomplicated phacoemulsification?. Ophthalmologica. 2003;217(6):408?412.
20. Yonekawa Y., Kim I.K. ?Pseudophakic cystoid macular edema?. Curr Opin Ophthalmol. 2012;23(1):26?32.
21. Kim S.J., Equi R., Bressler N.M. ?Analysis of macular edema after cataract surgery in patients with diabetes using optical coherence tomography?. Ophthalmology. 2007;114(5):881?889.
22. Lobo C.L., Faria P.M., Soares M.A., Bernardes R.C., Cunha-Vaz J.G. ?Macular alterations after small-incision cataract surgery?. J Cataract Refract Surg. 2004;30(4):752?760.
23. Wielders L.H.P., Lambermont V.A., Schouten J.S.A.G., et al. ?Prevention of cystoid macular edema after cataract surgery in nondiabetic and diabetic patients: a systematic review and meta-analysis?. Am J Ophthalmol. 2015;160(5):968?981.
tekst: Lek. Anna Bielecka | prof. dr hab. n. med. Jacek P. Szaflik | Samodzielny Publiczny Kliniczny Szpital Okulistyczny w Warszawie | Katedra i Klinika Okulistyki II Wydziału Lekarskiego Warszawskiego Uniwersytetu Medycznego