Nazwa leku, podmiot odpowiedzialny:
FIASP (insulinum aspartum) Novo Nordisk Pharma
Wskazanie do refundacji: cukrzyca typu 1.
Procedura refundacyjna: refundacja apteczna
Pozostałe wskazania (w tym refundowane): wnioskowany lek, zgodnie z Charakterystyką Produktu Leczniczego, jest wskazany do stosowania u dorosłych w leczeniu cukrzycy. Wnioskowane wskazanie (cukrzyca typu 1) mieści się we wskazaniu zarejestrowanym (cukrzyca u dorosłych). Jednak wnioskowane wskazanie potencjalnie rozszerza wskazanie rejestracyjne o populację pediatryczną.
Opis wnioskowanej technologii:
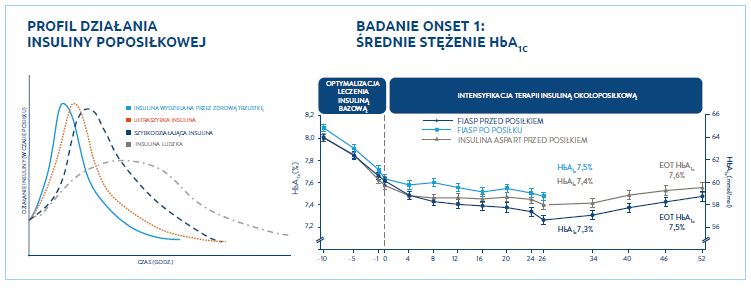
Produkt leczniczy Fiasp jest szybkodziałającą formą insuliny aspart, w przypadku której dodatek nikotynamidu powoduje szybsze początkowe wchłanianie insuliny, a dodatek niacynamidu modyfikuje absorpcję, podczas gdy dodatek L-argininy poprawia stabilność. Insuliny, w tym insulina aspart, wywierają swoje swoiste działanie przez wiązanie się z receptorami insulinowymi. Insulina związana z receptorem obniża stężenie glukozy we krwi poprzez ułatwienie wychwytu glukozy przez komórki mięśni szkieletowych i tkanki tłuszczowej oraz poprzez hamowanie uwalniania glukozy z wątroby. Insulina hamuje lipolizę w adipocytach, hamuje proteolizę i wzmaga syntezę białek. Podstawowym działaniem produktu leczniczego Fiasp jest regulowanie metabolizmu glukozy. Fiasp powoduje szybsze początkowe wchłanianie insuliny w porównaniu z insuliną aspart oraz szybszy początek działania niż inne analogi szybkodziałajace. Fiasp jest insuliną doposiłkową, podawaną podskórnie przed rozpoczęciem posiłku (Fiasp może zostać podany nawet bezpośrednio przed posiłkiem) lub do 20 minut po rozpoczęciu posiłku ? jest to szczególnie ważne w sytuacji, kiedy trudno jest przewidzieć wielkość i kaloryczność posiłku. Fiasp wykazuje lepszą skuteczność względem Novorapid w redukcji stężenia HbA1c, gdy jest stosowany przed posiłkiem, oraz porównywalną skuteczność przy podaniu po posiłku, przy zachowaniu profilu bezpieczeństwa oraz szybszy początek działania niż inne szybkodziałające analogi glukozy. W porównaniu z insuliną aspart Fiasp po podaniu sc. za pomocą pena wykazuje:
- 2-krotnie szybszy czas pojawienia się w surowicy,
- 2-krotnie wyższą ekspozycję na insulinę w ciągu pierwszych 30 min,
- 4-krotnie wyższą ekspozycję na insulinę w ciągu pierwszych 15 min,
- ponad 74% większe działanie hipoglikemizujące w ciągu pierwszych 30 min, w porównaniu z insuliną aspart Fiasp po podaniu w pompie insulinowej wykazuje ok. 3-krotnie wyższą ekspozycję na insulinę w ciągu pierwszych 30 min.
Problem zdrowotny:
Cukrzyca to grupa chorób metabolicznych, charakteryzujących się hiperglikemią wynikającą z defektu wydzielania lub działania insuliny. W Polsce na cukrzycę typu 1 choruje 6400 dzieci w wieku 0-14 lat oraz ok. 180 tys. osób powyżej 14 r.ż.
Leczenie i cele leczenia:
Odnalezione wytyczne wskazują, iż optymalnym standardem leczenia cukrzycy typu 1 jest insulinoterapia. Wytyczne zalecają schematy basal-bolus u dorosłych pacjentów z cukrzycą typu 1. Do insulin bolusowych zalicza się szybkodziałające analogii insulin (insulina aspart, insulina glargine, insulina lispro) i krótkodziałające insuliny. Zgodnie z opinią eksperta klinicznego w leczeniu cukrzycy typu 1 stosuje się: leczenie insuliną LAA (ang. long-acting insulin analogs, długodziałający analog insulin) w skojarzeniu z szybkodziałającym analogiem insuliny (bolus), lub leczenie insuliną NPH (ang. neutral protamine Hagedorn, insulina ludzka o przedłużonym uwalnianiu) w skojarzeniu z szybkodziałającą ludzką insuliną (bolus), lub insulinę analogową szybkodziałającą w pompie insulinowej.
Rozwiązania międzynarodowe:
Odnaleziono 4 rekomendacje postępowania klinicznego w leczeniu cukrzycy typu 1: Polskie Towarzystwo Diabetologiczne (PTD) 2019, Diabetes Canada (DC) 2018 TDM1 (Kanada), Diabetes UK Position Statements 2019 (Wielka Brytania), International Society for Pediatric and Adolescent Diabetes (ISPAD ? Danne) 2018 (międzynarodowe). Odnalezione wytyczne wskazują insulinoterapię jako optymalny standard leczenia cukrzycy typu 1 (PTD 2019, DC 2018, Diabetes UK Position Statements 2019, ISPAD 2018). Dodatkowo kanadyjskie wytyczne wymieniają insulinę aspart wśród szybkodziałających analogów insulin stosowanych jako insuliny bolusowe w leczeniu cukrzycy typu 1 u pacjentów dorosłych (DC 2018). Ponadto wskazują, iż szybciej działająca insulina aspart jest uwalniana szybciej niż insulina aspart. U pacjentów z cukrzycą typu 1 wykazano, że nie jest gorsza (ang. non-inferior) w zakresie redukcji stężenia HbA1c i lepsza w zakresie poposiłkowej kontroli glikemii.
Według międzynarodowych wytycznych ISPAD 2018 stworzonych dla populacji pediatrycznej, szybciej działająca insulina aspart jest szybciej uwalniana i bardziej stabilna niż insulina aspart, co oznacza, że powinna lepiej kontrolować poposiłkowe skoki stężenia glukozy we krwi i powodować mniej epizodów hipoglikemii po kilku godzinach od podania. U dzieci ma podobny profil farmakokinetyczny i farmakodynamiczny jak u pacjentów dorosłych, natomiast obecnie zarejestrowana jest tylko do stosowania u pacjentów dorosłych.
W wyniku wyszukiwania odnaleziono 5 rekomendacji refundacyjnych dotyczących stosowania produktu Fiasp: All Wales Medicines Strategy Group (AWMSG) 2017 (Walia) ? w sytuacji, gdy produkt leczniczy stanowi nową formulację refundowanego produktu leczniczego i generuje te same lub niższe koszty AWMSG odstępuje od oceny produktu leczniczego ? Fiasp spełnia te warunki względem produktu leczniczego NovoRapid, Scottish Medicines Consortium (SMC) 2017 ? rekomendacja pozytywna we wskazaniu: leczenie cukrzycy u dorosłych, Haute Autorité de Santé (HAS) 2017 (Francja) ? rekomendacja pozytywna we wskazaniu: leczenie cukrzycy u dorosłych, Pharmaceutical Benefits Advisory Committee (PBAC) 2018 (Australia) ? rekomendacja pozytywna we wskazaniu: leczenie cukrzycy u dorosłych, Tandv?rds-och läkemedelsförm?nsverket (TLV) 2017 (Szwecja) ? rekomendacja negatywna we wskazaniu: leczenie cukrzycy u dorosłych ze względu na zaproponowaną cenę produktu leczniczego.
Według informacji przedstawionych przez wnioskodawcę lek Fiasp jest refundowany:
- w postaci roztworu w 13 krajach UE i EFTA (na 31 wskazanych): Austria, Belgia, Czechy, Dania, Finlandia, Francja, Grecja, Holandia, Irlandia, Luksemburg, Norwegia, Szwajcaria, Wielka Brytania,
- w postaci wkładów Penfill w 14 krajach UE i EFTA (na 31 wskazanych): Austria, Czechy, Dania, Finlandia, Francja, Holandia, Irlandia, Islandia, Niemcy, Norwegia, Słowenia, Szwajcaria, Wielka Brytania, Włochy.
Więcej informacji :
http://bipold.aotm.gov.pl/assets/files/zlecenia_mz/2019/064/REK/RP_44_2019_Fiasp.pdf